Este artículo apareció originalmente en Undark.
Cuando la Organización Mundial de la Salud aprobó una vacuna contra la malaria por primera vez en octubre de 2021, fue ampliamente aclamada como un hito. “Este es un momento histórico”, dicho El director general de la OMS, Tedros Adhanom Ghebreyesus, en un comunicado ese mes.
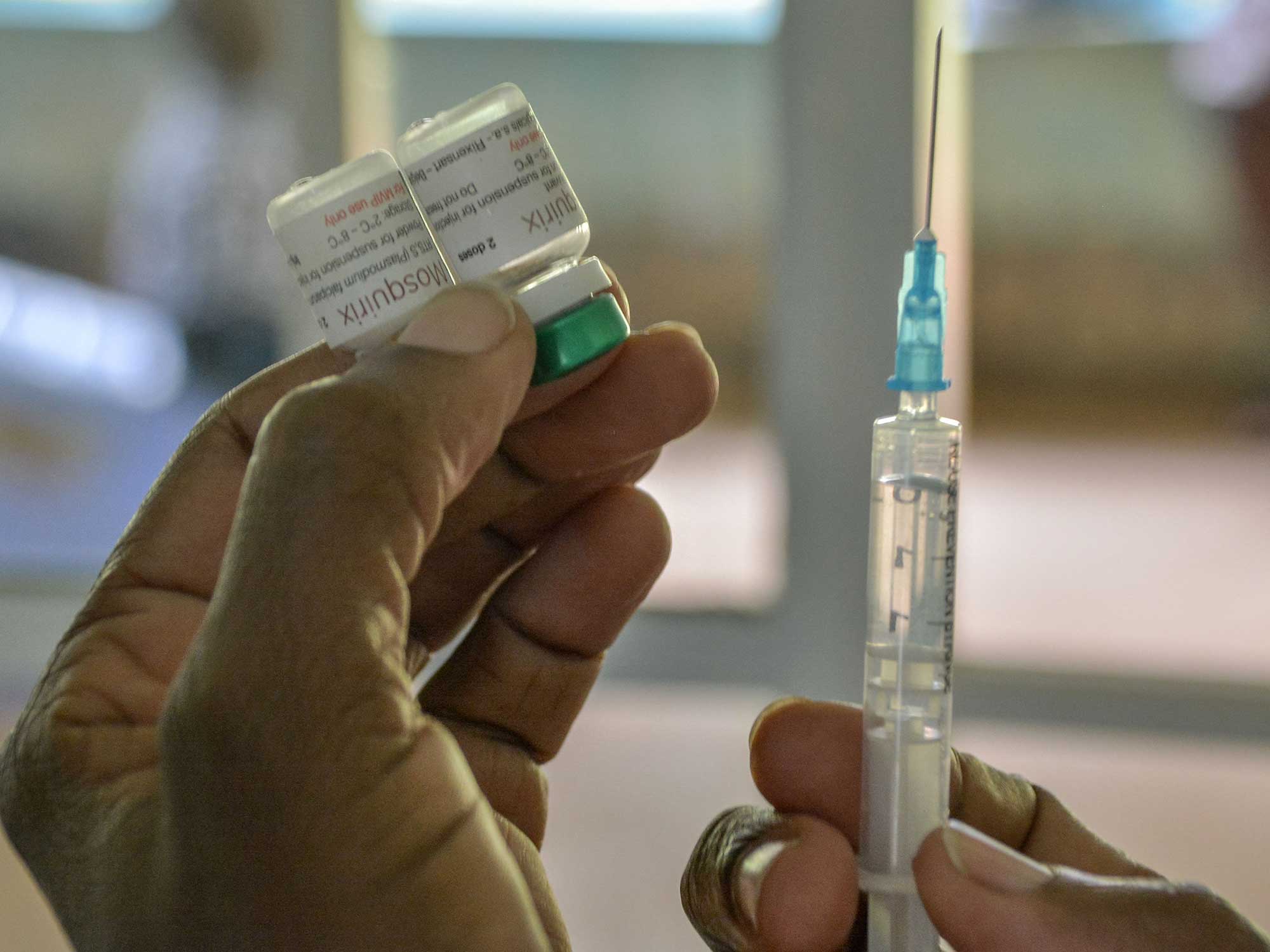
La vacuna, denominada RTS,S,promesas una reducción del 30 por ciento en la malaria grave en niños completamente vacunados. En 2020, un equipo de investigación estimado que cada año, la vacuna podría prevenir entre 3 y 10 millones de casos de malaria y salvar la vida de 14.000 a 51.000 niños pequeños, dependiendo de cómo se implemente.
Sin embargo, lo que esos aplausos a menudo no notaron fue que el ingrediente central de la vacuna pionera en realidad tenía casi 35 años, y que los investigadores sabían desde fines de la década de 1990 que la fórmula probablemente era algo efectiva para proteger contra la malaria.
En un momento en que las vacunas contra el covid-19 se desarrollaron y autorizaron en menos de un año, el retraso de la malaria plantea una pregunta: ¿por qué tardó tanto en llegar una vacuna para una de las principales causas de muerte a nivel mundial? Según los investigadores involucrados en el desarrollo de RTS,S, la respuesta involucra los desafíos de desarrollar una vacuna contra un molesto parásito, y la falta crónica de urgencia y financiamiento detrás de la investigación de la malaria, lo que obstaculizó la logística de los ensayos de investigación en cada paso.
Las personas afectadas por la malaria “no son europeos, no son australianos, son niños africanos pobres”, dijo Ashley Birkett, directora de la iniciativa de vacunas contra la malaria en PATH, una organización mundial de salud sin fines de lucro. “Desafortunadamente, creo que tenemos que aceptar que eso es parte de la razón de la falta de urgencia en la comunidad”.
Los investigadores habían estado buscando una vacuna contra la malaria desde finales de la década de 1960. En 1980, ellos identificado una proteína que abunda en la superficie del parásito, llamada proteína circumsporozoite, y se dio cuenta de que una vacuna dirigida contra esta proteína podría otorgar inmunidad. Después de que los investigadores del gobierno de EE. UU. secuenciado
El trabajo, recordaron los expertos, fue extremadamente desafiante. El parásito de la malaria tiene un ciclo de vida notoriamente complejo con al menos tres etapas distintas una vez que está dentro de los humanos, y “en realidad se está cambiando de ropa durante la evolución, durante el ciclo”, dijo Lode Schuerman, directora de asuntos científicos del programa de vacunas para la salud global de GSK. . Cualquier vacuna desarrollada contra una etapa en particular tendría que detener la infección en ese momento y no funcionaría si el parásito hubiera avanzado a la siguiente etapa. Además, aún no existían las herramientas básicas que los investigadores utilizan hoy para acelerar el desarrollo de vacunas.
Más de una docena de intentos de vacunas basados en la proteína circumsporozoite fracasaron. La excepción fue RTS,S. A fines de la década de 1980 y principios de la de 1990, el equipo descubrió varios detalles técnicos y una prueba de 1998 en Gambia, en la que participaron 250 hombres, fundar
“Ese fue realmente el comienzo de RTS,S”, dijo Brian Greenwood, un experto en enfermedades infecciosas de la Escuela de Higiene y Medicina Tropical de Londres que participó en el ensayo de Gambia.
Aún así, la atención a la vacuna, recordó Greenwood, fue impulsada más por el interés intelectual que por un sentido de urgencia médica, al menos para el público en general, más allá de las tropas estadounidenses. “No creo que haya ningún tipo de empujón. Fue hecho por personas más académicas e interesadas en la inmunología”, dijo. “No fue visto como un problema de salud pública”.
Y, según le dijeron a Undark las personas involucradas en el desarrollo de la vacuna, la vacuna prometedora estaba a punto de encontrarse con un conjunto completamente nuevo de problemas: la miríada de tribulaciones que conlleva probar una vacuna que no tiene un mercado comercial.
En 1999, Ripley Ballou, una vacunóloga que entonces trabajaba en el Instituto de Investigación del Ejército Walter Reed, voló a Europa para reunirse con ejecutivos de GSK. “Todavía estaba en el ejército en ese momento”, recordó, “y estábamos allí con nuestros uniformes en Bélgica”. En una sala de conferencias con mesas largas, Ballou y sus colegas de GSK se sentaron y presentaron sus hallazgos del ensayo de Gambia. “Tuvimos este rayo de esperanza que surgió de este estudio que dice, ‘sabes, qué, algo está sucediendo aquí, y creemos que realmente debemos llevarlo al siguiente paso’”, dijo. Y ese próximo paso sería probar la vacuna en el grupo que más se beneficiaría: los niños.
GSK accedió a seguir adelante, siempre que Ballou y sus colegas pudieran obtener algún financiamiento adicional de una organización asociada. Existía un alto riesgo de que el proyecto fracasara; incluso si tuviera éxito, GSK podría esperar una pequeña recompensa financiera. Y el ejército de EE. UU. ya no estaba interesado en RTS,S, sin estar convencido de que la eficacia haría lo suficiente para proteger a las tropas.
En cambio, la organización socia que financió el trabajo resultó ser la Iniciativa de Vacuna contra la Malaria en PATH establecida apenas un año antes a través de una subvención de la Fundación Bill y Melinda Gates.
“Dada la actitud hacia las vacunas a nivel mundial, era importante asegurarnos de descartar cualquier posible problema de seguridad”, dijo Wongani Nyangulu.
Cuando los fabricantes de vacunas comenzaron a lanzar ensayos en países africanos, pronto se dieron cuenta de que la tarea de probar la vacuna no sería nada fácil. Hubo muchos problemas logísticos, dijo Ballou. “Tuvimos que ir y había un edificio sin nada, solo una capa de concreto, y tuvimos que convertirlo en un laboratorio”, recordó. “Eso tomó tiempo, eso tomó dinero”.
Estos ensayos también estaban dirigidos a bebés y niños pequeños, por lo que los ensayos de Fase I y II, que analizan la seguridad y eficacia de la inyección, tuvieron que realizarse primero en adultos, luego en niños mayores y finalmente en niños pequeños, optimizando la dosis contra los efectos secundarios para cada grupo de edad antes de continuar. “Todo ese proceso tomó alrededor de 10 años”, dijo Greenwood.
el prometedor resultados de los ensayos de fase II, en los que los bebés experimentaron una reducción del 65,9 por ciento en la tasa de infección en comparación con el grupo de control en los meses posteriores a la tercera dosis, condujeron a un ensayo de fase III a gran escala, que no comenzó hasta 2009. Hubo una curva de aprendizaje empinada para diseñar el ensayo, dijo Ballou, “nadie había hecho nunca un ensayo de vacuna contra la malaria a esta escala”.
Los ensayos de fase III se llevaron a cabo entre 2009 y 2014 en siete países del África subsahariana. Inscribieron a más de 15.000 niños. Y los resultados fueron prometedores, tanto que GSK comenzó a preparar una planta de fabricación para la toma, según Schuerman.
Pero en octubre de 2015, una revisión de la OMS de los datos del ensayo de Fase III encontró que la tasa de meningitis era más alta en el grupo vacunado que en el control y que la muerte era más alta entre las niñas que habían recibido una vacuna, aunque no se sabía si estaba relacionado con la inyección. no está claro Para abordar estos problemas y probar la vacuna en un entorno más amplio de la vida real, la OMS solicitó un ensayo aún más grande. Este anuncio salió de la nada, dijeron varios científicos. “Tuvimos que cerrar y suspender todo el lado de la fabricación”, dijo Schuerman. En cambio, agregó, una vez más, el equipo de la vacuna se encargó del lento trabajo de establecer ensayos clínicos: buscar fondos, seleccionar países para la implementación y contratar personas para realizar el ensayo.
Hoy en día, la mayoría de los investigadores están de acuerdo en que el estudio adicional estaba justificado. “Dada la actitud hacia las vacunas a nivel mundial, era importante asegurarnos de descartar cualquier posible problema de seguridad”, dijo Wongani Nyangulu, médico que dirige un sitio de estudio de fase IV en el sur de Malawi.
Se necesitaron cuatro años para iniciar el juicio. Finalmente, 900.000 niños en Ghana, Malawi y Kenia recibieron la vacuna. Después de revisar los resultados, la OMS recomendado la vacuna para su uso generalizado en áreas de transmisión de malaria moderada a alta en octubre de 2021. En diciembre, GAVI, la agencia global que financia y distribuye vacunas en países pobres, Anunciado invertiría 155,7 millones de dólares en un despliegue de RTS,S.
Más de 20 años después de los primeros ensayos prometedores, RTS,S estaba listo para su uso generalizado.
Cuando se aprobó la RTS,S, ya se habían desarrollado y autorizado en todo el mundo vacunas para otro asesino mundial, el covid-19, menos de dos años después de que surgiera el virus.
Las aparentes disparidades han frustrado a algunos investigadores en el África subsahariana. “Si se dirigiera la misma energía y recursos hacia el desarrollo de una vacuna contra la malaria como ha sido el caso para el covid-19, entonces la malaria podría erradicarse”, escribió Damaris Matoke-Muhia, científica del Instituto de Investigación Médica de Kenia, en un artículo. ensayo para el sitio de desarrollo global SciDev.Net el pasado agosto. (En ese momento, señaló, la malaria estaba matando a más personas en el continente que el covid-19).
Otros investigadores africanos también han notado la discrepancia. Deus Ishengoma, un experto en malaria del Instituto Nacional de Investigación Médica de Tanzania, señaló que, teniendo en cuenta a Covid, sería “realmente malo si el mundo ahora cierra los ojos ante enfermedades como la malaria”. La velocidad de desarrollo de la vacuna contra el covid-19, agregó, significa que “nunca tendremos una justificación o excusa para no hacer una vacuna contra la malaria en los próximos 10 años”.
Otros expertos advirtieron que hacer comparaciones entre las vacunas no es del todo justo. “Covid es un objetivo mucho más fácil para una vacuna”, dijo Birkett, el ejecutivo de PATH. La malaria, agregó, “es probablemente un orden de magnitud más difícil”. La eficacia de RTS,S, dijeron varios expertos, probablemente también ralentizó el proceso. Y los medicamentos antipalúdicos y otras herramientas han ayudado durante mucho tiempo a compensar la carga de la malaria, dijo Birkett, por lo que la vacuna no era una prioridad en el mismo sentido en comparación con el covid-19.
Aún así, dijeron los expertos, la disparidad refleja patrones de larga data en los que las enfermedades mortales reciben atención y cuáles no. “Principalmente, este es el problema al que te enfrentas cuando intentas desarrollar una vacuna que nadie quiere pagar”, dijo Ballou.
Teniendo en cuenta a Covid, sería “realmente malo si el mundo ahora cierra los ojos ante enfermedades como la malaria”, dijo Deus Ishengoma.
Los problemas de financiación plagaron todos y cada uno de los pasos del desarrollo, dijo Birkett. “Tuvimos que ir muy secuencialmente, paso a paso, generar los datos, ir y recaudar el dinero, diseñar el protocolo”. Varios expertos temen que la escasez de fondos también obstaculice el lanzamiento de RTS,S. Este es el mayor riesgo que enfrenta el programa de vacunas en este momento, dijo Ballou. Los fondos para la investigación y el desarrollo de vacunas contra la malaria, especialmente para el desarrollo clínico, han tenido una tendencia a la baja desde 2017, y en 2020 se redujeron en $ 21 millones, una caída del 15 por ciento con respecto al año anterior. de acuerdo a a Policy Cures Research, un grupo de expertos en salud global.
Sin embargo, el desarrollo de RTS,S ha allanado el camino para la próxima generación de vacunas contra la malaria. La vacuna R21 de la Universidad de Oxford, que mostró una eficacia prometedora del 77 por ciento en los ensayos de fase II, es probablemente el siguiente en la línea. “Se beneficiarán enormemente del sistema de entrega y los reguladores, ya que todos están acostumbrados”, dijo Greenwood. Aún así, R21 podría no cambiar las reglas del juego, ya que se basa en la misma fórmula subyacente que RTS,S, dijo Birkett, y “todos los datos sugieren que, hasta ahora, será muy similar”.
En julio de 2021, BioNTech, una empresa de biotecnología alemana que cocreó la primera vacuna de ARNm contra el covid-19, también anunció planes para utilizar la misma tecnología para desarrollar una vacuna contra la malaria, con ensayos clínicos previstos para 2022.
La próxima ronda de vacunas, en caso de que resulten seguras y más eficaces, tardará mucho menos de 35 años en llegar al mercado. “Estoy muy seguro”, dijo Birkett, “de que podemos ir más rápido la próxima vez”.
